
医療分野のPVC(ポリ塩化ビニル)の動向と代替樹脂について
軟質ポリ塩化ビニル(PVC)は、化学的安定性と優れた柔軟性・耐久性から、輸液バッグ、輸液チューブ、血液バッグなど医療現場で広く使用されていますが、使用されている可塑剤の溶出等による安全性への懸念から軟質PVCの使用を見直す動きがあります。一方で、材料変更に伴い従来の接合方法が適用できず、他部材とのアッセンブリが課題となるケースも少なくありません。本記事では、PVCを取り巻く課題や規制動向を整理するとともに、三菱ケミカルが提供する材料を含めたPVC代替樹脂と、アッセンブリ方法まで含めて技術解説をいたします。
医療用途におけるPVC使用の主な懸念
可塑剤(DEHP)溶出による健康への懸念
軟質PVCは、柔軟性付与のために可塑剤が添加されますが、可塑剤の中でもDEHP(フタル酸ジ-2-エチルヘキシル)は血液や脂溶性薬液との接触により溶出することが報告されています。
日本では、平成14年(2002年)、厚生労働省が医療機関に対し、PVC製医療用具からのDEHP溶出に関する通知を発出しました。新生児・乳児に使用されるフィーディングチューブについては、早期の使用中止と代替品への切り替えが推奨されている他、感受性が高い患者に対しては、優先的に代替品に切り替えるよう配慮が求められています。1)
また、EUでDEHPは「生殖毒性1B物質」として分類されていますが、2023年11月のREACH改正に伴い、医療機器における DEHP使用期限が改正されています。(申請期限:2029年1月1日、使用期限:2030年7月1日) 2)
また、米国カリフォルニア州では「Toxic-Free Medical Devices Act」により、2030年以降、特定の医療機器でDEHP使用を禁止する方向性が示されるなど、規制・立法の動きも進んでいます。3)
薬効成分吸着による含量低下の懸念
健康リスクのみならず、期待した薬効が十分に得られなくなる例も報告されています。軟質PVCの表面および可塑剤は疎水性であるため、特に脂溶性の高い薬剤(インスリン、ニトログリセリン、ジアゼパム)がチューブ内面に吸着しやすく、顕著な含量低下を招きます。実際の患者への投与量の低下やばらつきにつながるため、吸着の少ないチューブ材への切り替えが検討されています。4)5)
軟質PVC代替樹脂
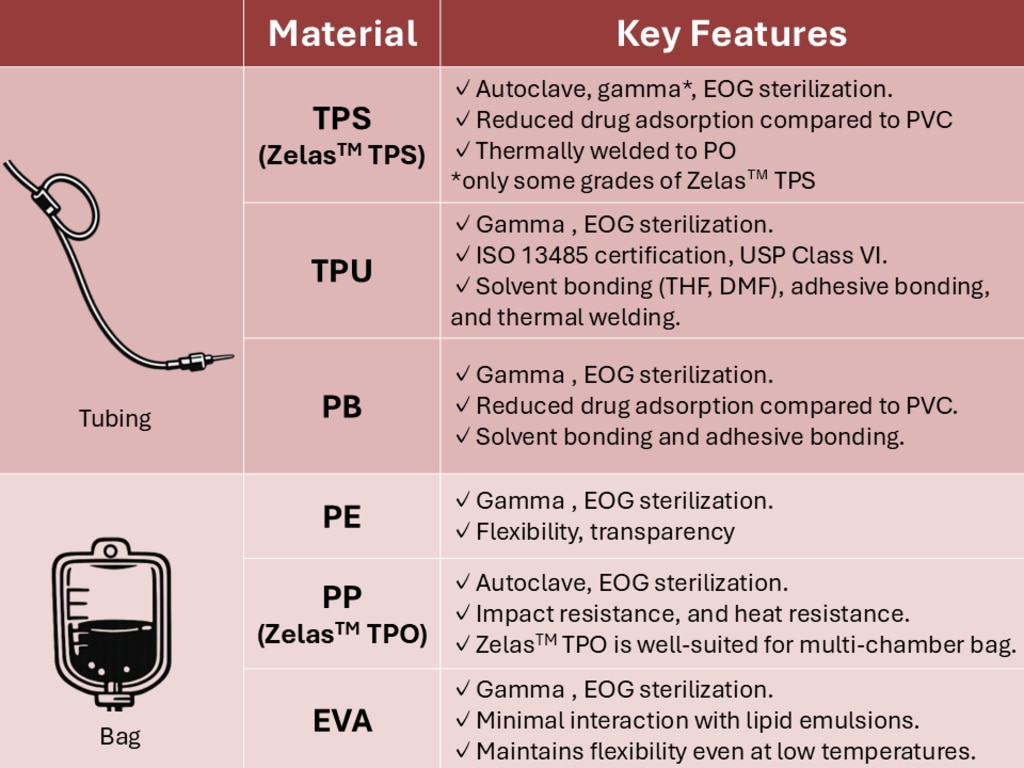
TPS(スチレン系熱可塑性エラストマー)
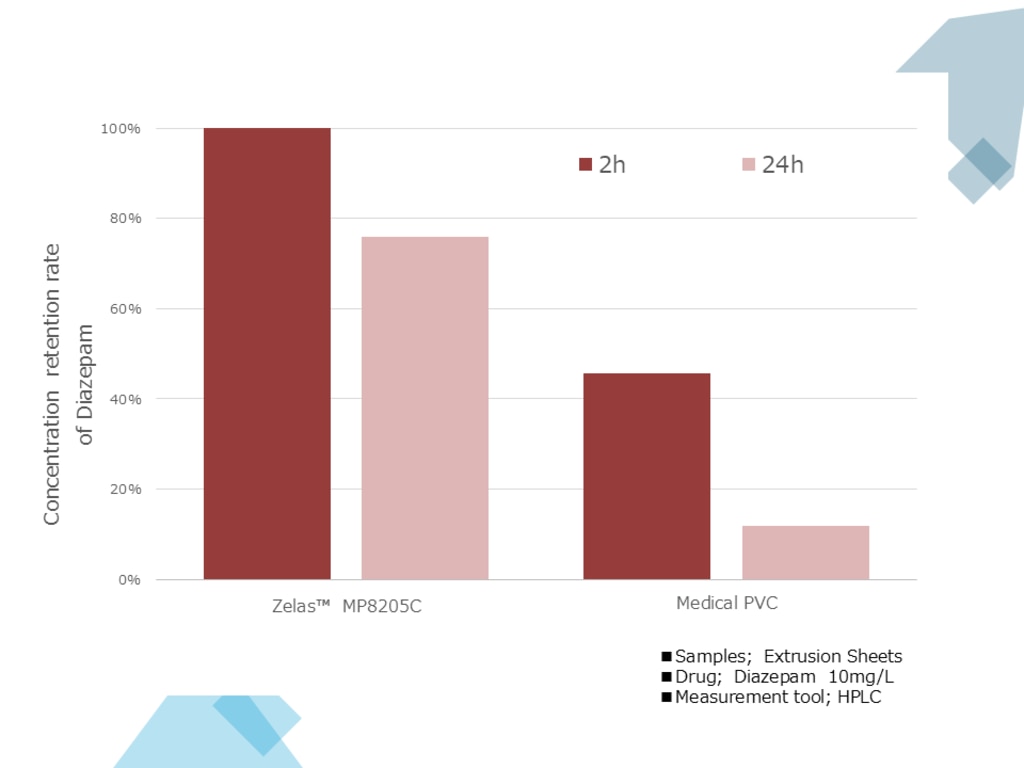
TPSは、良好なゴム弾性を有するスチレン系熱可塑性エラストマーで、衛生性も高いことからチューブ、ガスケット、ゴム栓など幅広く医療分野に使用されています。三菱ケミカルのZelas™TPS(MP8205C)では、抗不安薬として知られるジアゼパム(ベンソジアゼピン誘導体)における吸着試験において、PVCと比べて高い濃度保持率を維持したという結果が得られており(下図)、薬効を損なわない医療用チューブとしての活用が期待されます。また、三菱ケミカルでは、γ線滅菌(25kGy)後も溶出物が少ない次世代のチューブグレード(Zelas™MP6301C)も開発し、輸液チューブなどディスポーザブル製品の包装後最終滅菌を可能にします。
主な特徴:
• 各種滅菌方法(オートクレーブ、ガンマ線、EOG)への対応グレードあり
• 薬剤吸着量を従来PVC比で低減
• PP (ポリプロピレン)と熱で溶着が可能であり、超音波溶着やレーザー溶着にも対応
TPU(熱可塑性ポリウレタン)
TPUは、優れた機械的強度と柔軟性を備える熱可塑性ポリウレタンエラストマーで、生体適合性も高いことから、カテーテルやインプラントなど長期体内留置デバイスにも使用されています。
三菱ケミカルでは、ChronoFlex™ (カーボネート系)やChronoThane™(エーテル系)をはじめとするTPU製品をラインナップし、高付加価値医療機器市場向けへ展開しています。
主な特徴:
• ガンマ線滅菌、EOG滅菌に対応
• ISO 13485認証取得のもとで生産・開発し、USP Class VIをはじめとする各種生物学的安全性評価に適合
• 溶剤接着(THF、DMF、シクロヘキサノン)、接着剤接合、熱溶着可能
PB(ポリブタジエン)
PBは、1,2-ポリブタジエンを主成分とし、良好な柔軟性と機械的強度を有しながら薬剤非吸着性にも優れているため、医療用チューブ材料として用いられています。
主な特徴:
• γ線滅菌、EOG滅菌に対応
• 脂溶性薬剤に対して優れた非吸着性
• 溶剤接着や接着剤接合が用いられるが、表面処理により接着性を向上させることが推奨される場合あり
PE(ポリエチレン)
PE(ポリエチレン)は、医療分野で古くから使用されてきた代表的なポリオレフィンであり、低密度ポリエチレン(LDPE)や直鎖状低密度ポリエチレン(LLDPE)は柔軟性と耐応力割れ性に優れています。多層構造の一層として組み合わせることで、薬剤適合性・柔軟性・シール性などのバランスを最適化することができます。
主な特徴:
• γ線滅菌、EOG滅菌に対応 (オートクレーブ滅菌は×)
• 接着剤/溶剤接着は基本的には難しいが、ポリオレフィンとは熱溶着可能(超音波溶着やレーザー溶着も可)
PP(ポリプロピレン)
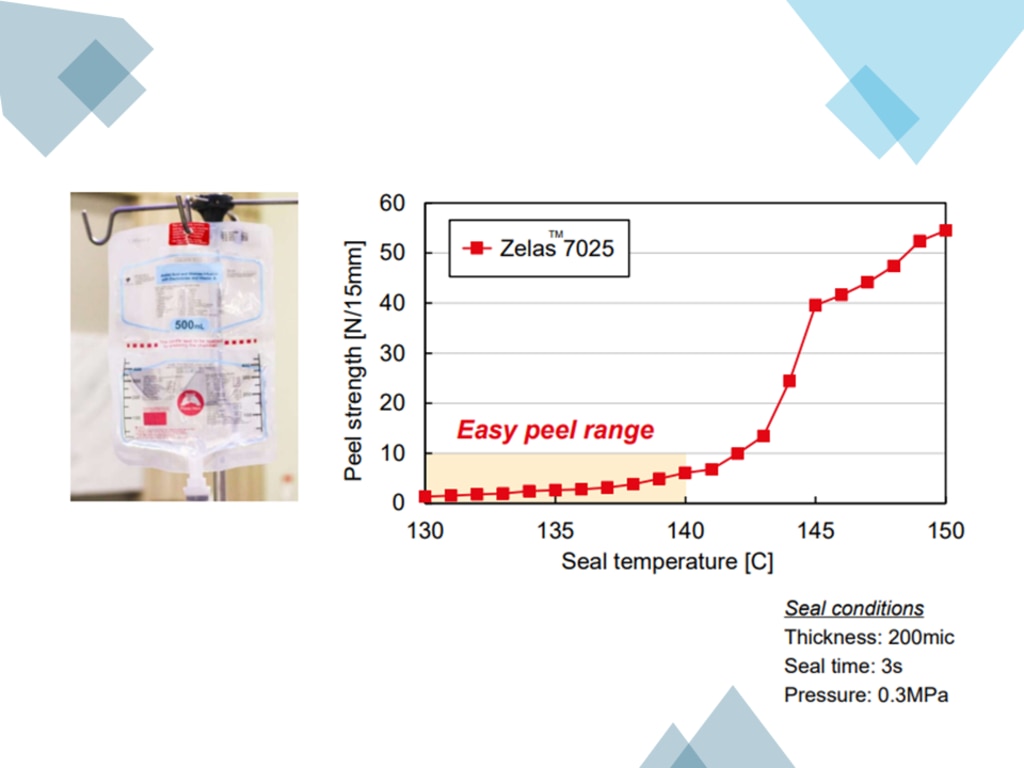
PP(ポリプロピレン)は、耐熱性と耐薬品性に優れ、主にオートクレーブ滅菌が求められるバッグに使用されます。三菱ケミカルのZelas™ TPOは、医療向けの熱可塑性オレフィン系エラストマーコンパウンドで、PPの耐熱性・耐薬品性を維持しつつ、ゴム弾性や柔軟性を付与した材料設計を行っています。特にZelas™7025は、ヒートシール温度によってシール強度を制御できることから、複室バッグの内層に好適です(下図)。Zelas™TPOでは内層以外にも、中間層・粘着層、外層の 各層に適したグレードを用意し、豊富な実績を有しています。
主な特徴:
• オートクレーブ滅菌、EOG滅菌に対応 (γ線滅菌は×)
• 優れた柔軟性・透明性・耐衝撃性・耐熱性
• 接着剤/溶剤接着は基本的には難しいが、ポリオレフィンとは熱溶着可能(超音波溶着やレーザー溶着も可)
EVA(エチレン・酢酸ビニル共重合体)
EVAは、エチレン・酢酸ビニル共重合体で、特にTPN(全静脈栄養)用IVバッグ材料として多くの実績があります。
主な特徴:
• γ線・EOG滅菌向けグレードが存在
• 脂肪乳剤との相互作用が少ない
• 低温でも柔軟性がある
ガス透過性が比較的大きいため、酸素や水蒸気バリアが要求される用途では、PPやCOC/COPとの多層化が検討されます。
PVC代替材料をご検討なら
健康リスクや含量低下への懸念からPVCを他材料へ置き換える動きが進んでいますが、PVCは高周波ウェルダや接着剤接着といった特有のアッセンブリ方法が確立されているため、代替材料への変更時に「どのように接合すればよいか」という課題に直面するケースも少なくありません。
三菱ケミカルでは、PVC代替材料の提供にとどまらず、それらに適したアッセンブリ方法に関する技術データも幅広く取り揃えています。材料選定から加工・接合方法まで、用途や課題に応じた具体的なご提案が可能です。PVC代替をご検討の際は、ぜひお気軽にご相談ください。
<注意事項>
本記事に掲載された情報は、公開時点で入手可能な情報源に基づき作成されておりますが、その正確性、完全性、最新性について、当社は一切の保証を行いません。使用用途に対する品質適性・安全性・適法性については、貴社にてご評価・ご判断をお願いします。
記載された材料特性、滅菌対応、加工性等の情報は、すべてのグレードや使用条件において同等の性能を保証するものではありません。適性については、貴社製品にてご評価・ご判断をお願いいたします。
参考文献
1)独立行政法人医薬品医療機器総合機構,医薬安発第1017002号”ポリ塩化ビニル製の医療用具から溶出する可塑剤(DEHP)について https://www.pmda.go.jp/safety/info-services/devices/0116.html
2)European Commission. Commission Regulation (EU) 2023/2482 of 13 November 2023 amending Regulation (EC) No 1907/2006 of the European Parliament and of the Council as regards the substance bis(2-ethylhexyl) phthalate (DEHP) in medical devices. Official Journal of the European Union, L 2023/2482, 14 November 2023. https://eur-lex.europa.eu/eli/reg/2023/2482/oj
3)California State Legislature. Assembly Bill No. 2300, Chapter 562: Medical devices: Di-(2-ethylhexyl) phthalate (DEHP). Approved by Governor September 25, 2024. California Health and Safety Code, Division 104, Part 3, Chapter 18, Sections 109050-109052. https://leginfo.legislature.ca.gov/faces/billNavClient.xhtml?bill_id=202320240AB2300
4)Treleano, A. ; Wolz, G.; Brandsch, R.; Welle, F. Int. J. Pharm., 2009, 369, 30-37.
5) Baker, R. C.; Josephson, R. L. Drug Intell. Clin. Pharm., 1983, 17, 726–731.




